全球首个能阻止阿尔茨海默病进展的药物获美国FDA加速审批上市
重磅!全球首个能阻止阿尔茨海默病进展的药物获美国FDA加速审批上市,时隔18年AD患者终获新药2021年06月08日 08:40 新浪财经综合新浪财经APP缩小字体放大字体收藏微博微信分享[iframe][/iframe] 安装新浪财经客户端第一时间接收最全面的市场资讯→【下载地址】
文章来源:奇点网
今天注定会被载入人类抗击阿尔茨海默病(AD)的史册。
美国时间6月7日,FDA加速审批渤健生物单抗药物Aducanumab上市,用于治疗AD。
这是自2003年以来,FDA批准的首款AD新药,也是自阿尔茨海默病被命名100多年来,首款获批的疾病修正类药物。
至此,人类结束了无法从根本上阻挡AD疾病进展的沧桑历史。
200多年前,当法国著名医生,拿破仑私人医生Philippe Pinel 和他的得意门生Jean Etienne Esquirol首次将老年性痴呆与其他痴呆分开时,人类对AD还知之甚少。
100多年前,当Alois Alzheimer 首次通过解剖发现AD患者大脑内存在淀粉样斑块和神经原纤维缠结时,人类对AD仍然知之甚少。
30多年前,首款AD药物进入临床试验,在随后的十余年时间里,FDA批准了5款治疗AD的药物,但这些药无一例外都是症状缓解类药物,对于AD疾病进展无能为力。站在这个历史节点,人类对AD依旧知之甚少。
30多年后的今天,首款可以阻止AD进展的疾病修正类药物终于获批上市。虽然AD的迷局人类仍然没有看清,但至少,我们站在了一个新的起点上。
200年间,AD从一个鲜为人知的疾病,成为影响全球数千万人的迷失梦魇。据统计,2019年,全球痴呆症患者数量高达5000万,到了2050年,这一人数还将增至1.5亿。同时据估计,到2030年,AD导致的经济负担将达到25亿美元,而到了2050年,这一数字将达到91亿美元。
与此同时,百余款潜在新药葬身于AD药物研发的天坑,从1998年到2017年,就有146款药物坠入天坑。但是面对迷失的深渊,人类不会退缩,因为我们没有退路。
黑暗中有一颗星亮起
Aducanumab登场时一鸣惊人。
2016年9月1日,享誉世界的顶级期刊《自然》在封面出现了两个醒目的大写单词:TARGETING AMYLOID,似乎在宣告一个振奋人心的新时代的到来。
图片来源:参考文献 当期的封面文章展示了一项激动人心的结果:靶向β淀粉样蛋白(Aβ)的全人源单抗药物Aducanumab在Ib期的PRIME研究中显示,可以有效降低患者大脑中的淀粉样斑块,且呈现剂量和时间依赖性。同时,Aducanumab在治疗1年后可延缓认知衰退,疗效呈剂量依赖性。
这是有史以来第一款能够减少AD患者大脑中Aβ,同时又可以延缓认知衰退的药物。经历了漫长至暗时刻的淀粉样蛋白假说终于出现了罕见的光明。
与此同时,Aducanumab的两项三期研究正在紧罗密布地开展。ENGAGE和EMERGE两项研究招募了2700例早期AD患者,临床主要终点为第18个月时的CDR-SB。
图片来源:upsplash 但事情并非一帆风顺。
2018年12月,入组患者完成了18个月治疗,随后基于无效性分析结果,两项三期试验于2019年3月21日宣布终止。久违的希望似乎又要破灭了。
然而就在试验终止后的7个月,2019年10月,渤健宣布,结合更大数据集的重新分析推翻了此前的无效性分析结果。
针对更大数据集的分析发现,EMERGE研究的高剂量组达到了主要终点,即在第78周,Aducanumab高剂量组的CDR-SB评分较安慰剂显著降低。
EMERGE研究的高剂量组还显示,患者在第78周时较基线可延缓临床进展;患者在认知方面(如记忆、定向力和语言)具有显著获益。患者在日常生活能力方面,如管理个人财务、做家务(打扫,购物,洗衣服)和独立出门旅行方面也具有获益。
不久之后,渤健向FDA提交了Aducanumab的上市申请。2020年8月7日,美国FDA宣布Aducanumab生物制剂许可申请(BLA)获得优先审查。此后,经过10个月的焦灼之后,FDA终于在今天宣布Aducanumab获得上市批准。
靶向Aβ:千帆折戟,但仍生机勃勃
100多年前,Alois Alzheimer 通过显微镜看到AD患者大脑中两种异常蛋白沉积:细胞外的β淀粉样蛋白斑块以及细胞内的神经原纤维缠结。正是这历史性的一瞥开启了AD疾病分子研究的序幕。
1984年,美国加州大学圣地亚哥分校的病理学家George Glenner 分离出了β淀粉样蛋白。此后,George Glenner 和同事Caine Wong 的研究提示,β淀粉样蛋白可能是由一种更大的蛋白被切割而产生的。
3年后他们的预测就得到了证实。1987年,德国科隆大学的科学家在顶级期刊《自然》上发表文章,宣布他们在21号染色体上发现了一种与遗传性阿尔茨海默病相关的基因,即淀粉样蛋白前体蛋白(APP)基因。此时,AD发病机制的淀粉样蛋白假说开始萌芽,但还没有受到广泛的认可。
淀粉样蛋白假说(图片来源:参考文献) 现在我们知道,β淀粉样蛋白是由淀粉样蛋白前体蛋白(APP)依序水解产生的。APP是一种跨膜蛋白,在许多人体组织中都有表达,尤其是在神经元突触中大量表达。
人类的APP可以通过两种不同的途径加工,分别为淀粉样蛋白途径和非淀粉样蛋白途径。在APP的淀粉样蛋白加工过程中,β-分泌酶首先将APP切割成膜连接的C端片段β(CTFβ或C99)和N端sAPPβ。
随后,CTFβ被γ-分泌酶切割成结构域AICD和一系列氨基酸片段。这些氨基酸片段会被进一步水解加工成β淀粉样蛋白最终形式:含40个氨基酸的Aβ40和含42个氨基酸的Aβ42。
APP两种不同的加工路径(图片来源:参考文献) 奠定淀粉样蛋白假说基石的证据来自于对家族性AD的深入研究。1991年,由Hardy领衔的研究团队发现了第一个可以导致家族性AD的APP基因突变。
5年后,其他两种导致家族性AD的基因突变也被发现:编码γ分泌酶复合体亚基的PSEN1 和PSEN2错义突变,会导致APP水解过程中产生更多Aβ42。此外,有关21三体综合征(唐氏综合征)和ApoE4等位基因的研究也都强有力地支持淀粉样蛋白假说。
APP两种不同的切割位点(图片来源:参考文献) 虽然目前已经有大量证据支持淀粉样蛋白假说,但让假说变成真理的方式只有一个:证明靶向Aβ的药物可以延缓AD的疾病进展。
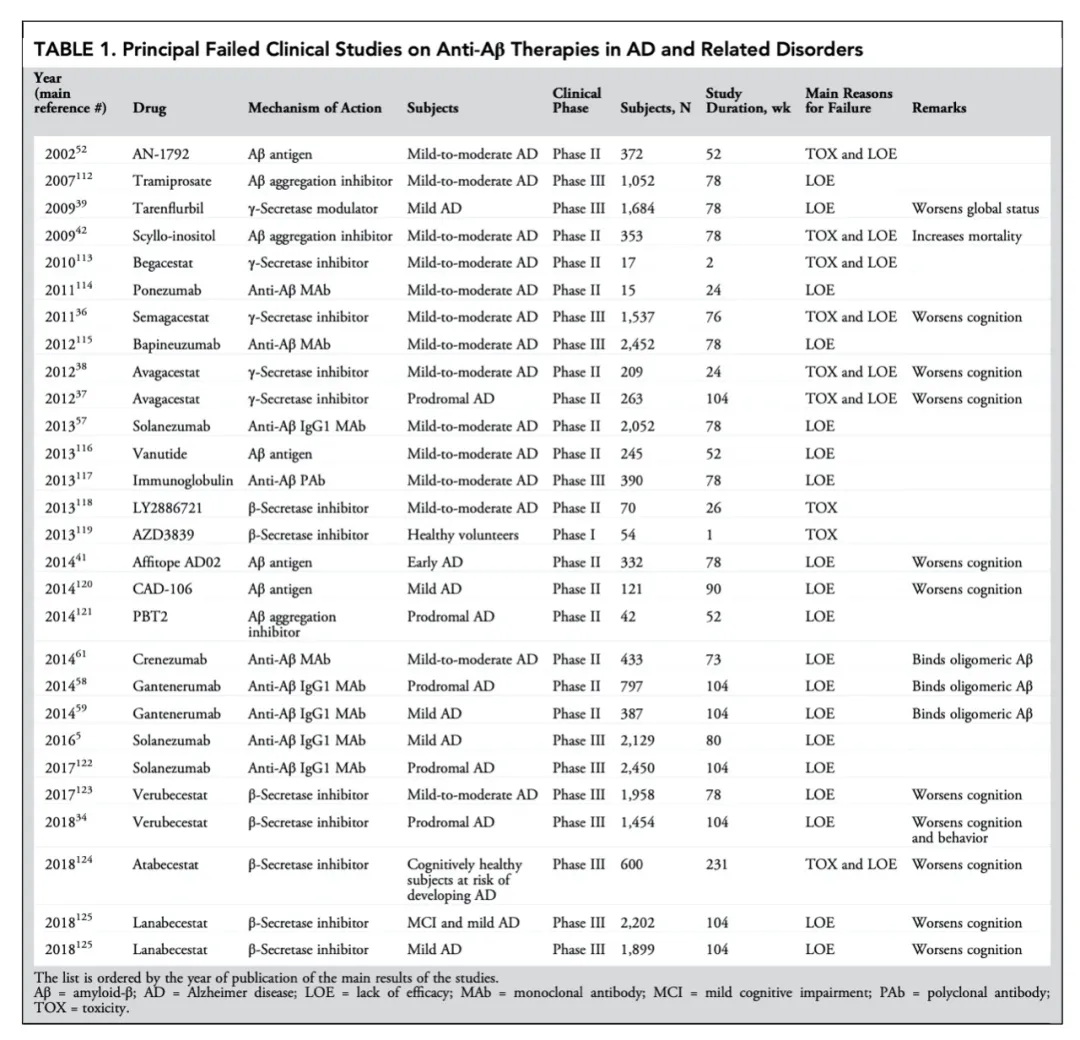
然而,这条路布满了荆棘。不管是致力于清除Aβ的免疫疗法,还是各种降低Aβ产生和聚集的疗法都相继坠入天坑。
2002年,首款靶向Aβ的免疫疗法宣告失败,在这项试验中6%的参与者出现了大脑和脑膜炎症。2011年,首个进入临床三期的γ分泌酶抑制剂Semagacestat遭遇惨败,这种药物不但使患者皮肤癌的发病率升高,而且还加重了认知障碍。
2012年,礼来(222.52, 20.50, 10.15%)公司的单抗药物Solanezumab治疗轻度到中度AD患者的两项三期研究Expedition1和Expedition2宣告失败,淀粉样蛋白假说再遭重创。
靶向Aβ药物失败的临床研究(图片来源:参考文献) 接连的失败促使科学家开始反思这些研究。对于某些研究,失败的主因在于药物本身。以γ分泌酶抑制剂Semagacestat为例,γ分泌酶除了切割APP之外,还负责切割各种其他类型的蛋白,简单地抑制γ分泌酶必然会引起各种各样的副作用。
除此之外,一个最为主流的判断认为:不是药不行,是治得太晚了。Aβ的沉积在AD症状出现之前的10~20年就已经出现,当疾病发展到痴呆阶段时再治疗为时已晚。
图片来源:veer 回应这种猜测的是Expedition1和Expedition2 两项试验的亚组分析,分析显示,轻度AD患者具有明显的认知改善。基于此,礼来公司又启动了针对轻度AD患者的Expedition3 三期研究。
然而,希望再次破灭。在2016年的CTAD大会上,礼来宣布Expedition3 试验没有达到预期终点。两年后,这项研究的数据发表在了NEJM上。
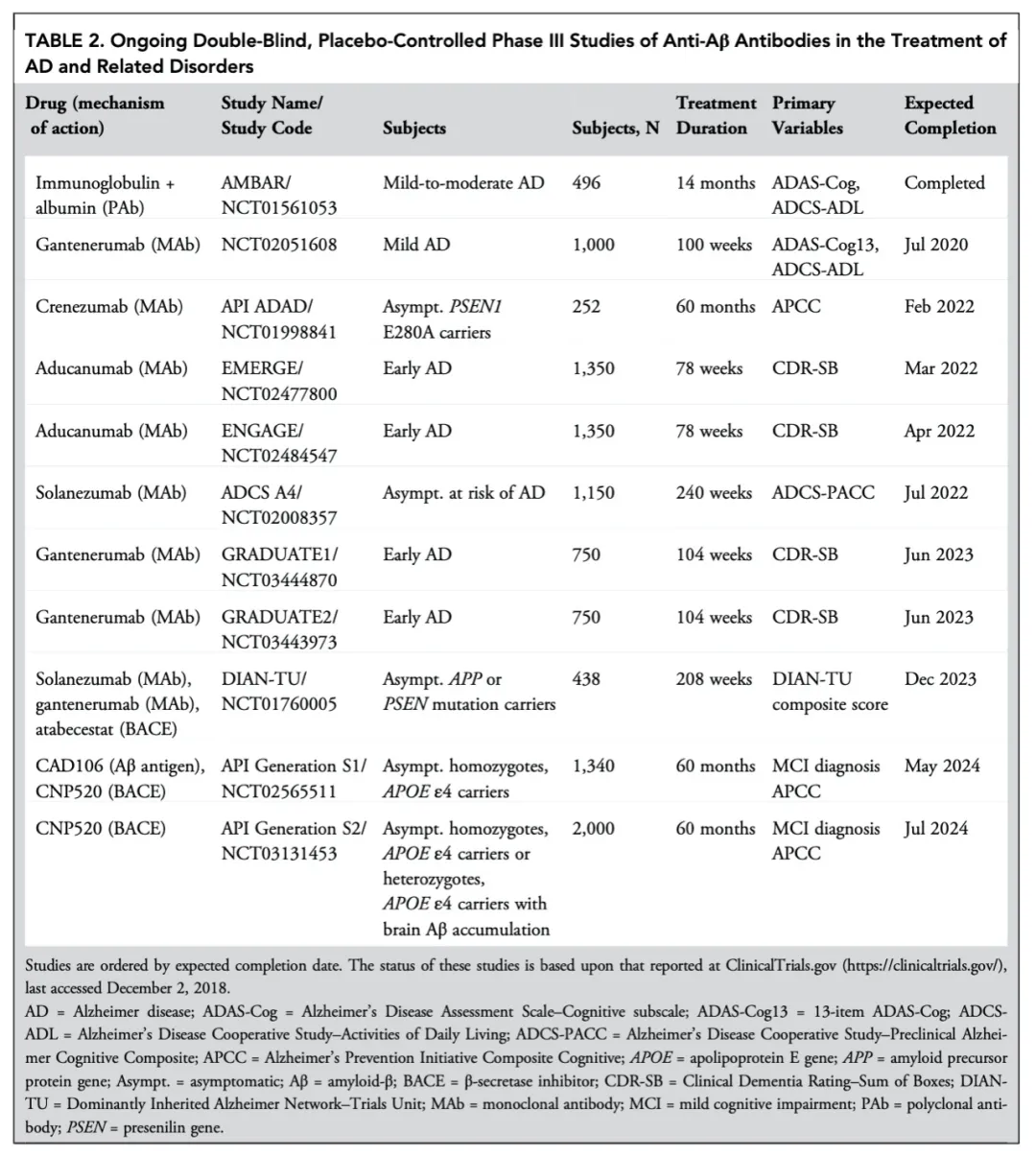
一次又一次的失败并没有浇灭科学界对于淀粉样蛋白理论的信心。目前仍然有大量靶向Aβ的药物正在进行临床试验,其中绝大部分针对轻度AD,以及AD源性MCI。也有研究将疾病干预的阶段推向预防,在家族性AD患者中验证靶向Aβ能否延缓AD的发生。
截止2018年仍在进行的靶向Aβ的临床研究(图片来源:参考文献) 在淀粉样蛋白假设跌宕起伏的30年里,Aducanumab最终成为那个可以远航的风帆。
走出迷雾的森林,到田野里去
尽管在Aducanumab获批之前,FDA有18年的时间没有批准任何AD新药上市;尽管在过去的20年里,有百余款新药落入天坑,但是人类始终没有放弃。
攻破AD不仅是一种紧迫而强烈的现实需求,也成了科学家探索生命未知的一种倔强。
2020年,clinicaltrials.gov. 上登记注册的AD临床研究就有121项。其中,疾病修正类生物疗法和疾病修正类小分子药物,以及症状缓解类小分子药物平分秋色。
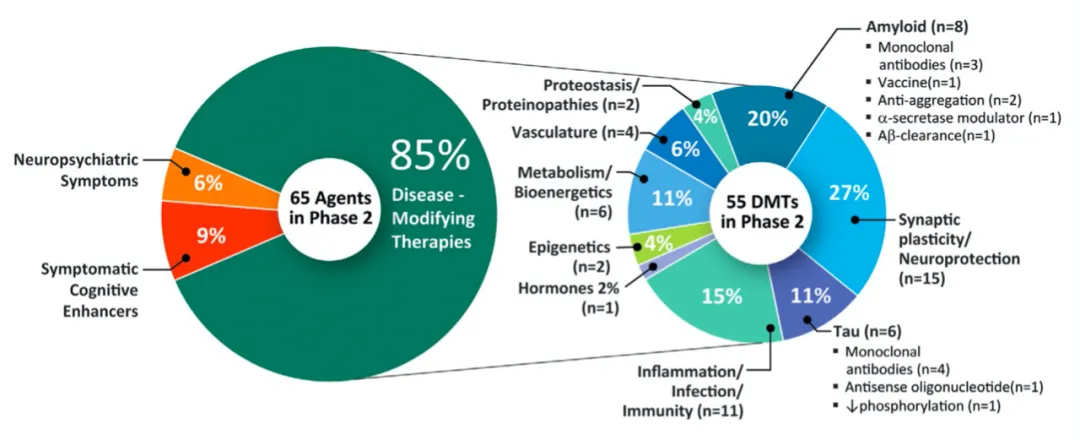
2020年,clinicaltrials.gov.上登记注册的AD临床研究(图片来源:参考文献) 在29个进入三期临床的药物中,59%为疾病修正类药物。而在这些疾病修正类药物中,有35%靶向Aβ,18%靶向炎症、感染和免疫,6%靶向tau蛋白。
图片来源:参考文献 而在55个进入二期临床的疾病修正类药物中,靶向Aβ的药物仅占20%,突触可塑性及神经保护类药物跃居第一位,占27%;靶向炎症、感染和免疫的药物热度依旧,占据了15%;而靶向tau蛋白的药物比重大增,占据11%。
图片来源:参考文献 这表明,AD药物的研发不再严重聚焦Aβ,而是向着更为广阔的田野进发。
希望下一个十年,我们可以彻底破解这迷失的梦魇。

内容来自网友分享,若违规或者侵犯您的权益,请联系我们
所有跟帖: ( 主贴楼主有权删除不文明回复,拉黑不受欢迎的用户 )
进入内容页点击屏幕右上分享按钮
楼主前期社区热帖:
- 关于回避型依恋,这一篇就够了 08/04/22
- 外交部回应G7和欧盟外长声明:列强梦应该醒醒了! 08/04/22
- 长剑-10和长剑-20巡航导弹有什么区别?长剑-100又是什么导弹? 08/04/22
- 《财富》世界500强:145家中国公司上榜,中企营收占比首超美国 08/03/22
- 国产大飞机距离交付有多远? 08/03/22
- ?谷爱凌问了一个很高尚的问题? 06/02/22
- ?三个字读错俩 06/01/22
- 巴西前部长:中国威胁谁了? 05/13/22
- 听歌 - 想某人 05/13/22
- ?岁月催人老,风定落花香? 04/25/22
- Elon Musk talks Twitter, Tesla and more live at TED2022 04/16/22
- ?俄乌战争启示 - 破窗 ? 04/08/22
- 西方叙事造成隔阂,中国舆论如何先发制人? 04/02/22
- 台媒称在美国施压下,台湾将恢复一年役期征兵制,释放了哪些信息? 03/29/22
- 骇人听闻的石墨炸弹,不杀人但可摧毁抵抗意志,有办法防范吗? 03/29/22
- 欧美发布芯片法案加剧全球半导体竞争 03/25/22
- From spy to president: The rise of Vladimir Putin 03/19/22
- 20分钟详解 - 俄罗斯经济到底是怎么回事儿? 03/19/22
- 霍布斯及其《利维坦》 03/10/22
- 《人类简史:从动物到上帝》第八章 历史从无正义 (节选) 03/10/22
>>>>查看更多楼主社区动态...